
Ŕ la mi-Aoűt, la province du Fujian et Drug Administration en 2019 pour informer la qualité de la médecine traditionnelle chinoise Des morceaux de concentration et de contrôle (processus de production) inspection spéciale et les conditions de manutention. Zhangzhou Pien Tze Huang Pharmaceutical Co., Ltd, Fujian Pine Ltd et d'autres 31 Pičces d'entreprises de production de la médecine chinoise en raison des défauts a été ordonné la rectification, oů les montagnes Rocheuses (Fuzhou) Pharmaceutical Co., Ltd est retirée en raison de graves lacunes certificat GMP. Au cours de Avril 2019 Juillet, la province du Fujian et Drug Administration pour organiser la concentration de la province et le contrôle de la qualité de la médecine ŕ base de plantes chinoises (procédés de production) d'inspection spéciale, l'examen a révélé que 31 entreprises dans la gestion des défauts existent en général, et plus d'entreprises question 14 il y a un défaut. Dont 16 entreprises produisant des défauts majeurs, les grands projets de défauts sont 1-2 gamme.
Parmi eux, le Rocky Mountain (Fuzhou) Pharmaceutical Co., Ltd est sérieusement une imparfaite, un inconvénient majeur, défaut général 9, conformément aux dispositions de la « approche de gestion de la certification des bonnes pratiques de fabrication » et « mesures de supervision et de gestion de production de drogue », Fujian administration provinciale des médicaments a identifié la montagne Rocky (Fuzhou) Pharmaceutical Co., Ltd ne répond pas ŕ l'évaluation des normes médicaments de certification GMP, donc en fonction de récupérer (systčme net, systčme de coupe) « certificat BPF des médicaments » de la société Pičces de la médecine chinoise. Le chčque a été trouvé fabricants de médicaments défectueux impliqués dans plusieurs sociétés connues et telles que Pékin Tongrentang Santé Pharmaceutical (Fuzhou) Co., Ltd général, il y a un défaut 9;
La présence de Zhangzhou Pien Tze Huang Pharmaceutical Co., Ltd. défaut général 5; présence Fujian Guizhen Tang Pharmaceutical Co., Ltd. défaut général 6, il y a un défaut majeur Xianzhi Technology (Fujian) Co., Ltd., défauts généraux 8.
Selon « inspection site production de drogues lignes directrices d'évaluation des risques », les services de réglementation des médicaments en vertu de la « bonnes pratiques de fabrication » (appelée GMP), aprčs une évaluation des risques, l'inspection sur place a constaté les entreprises de défauts sont généralement divisés en défauts graves, les principaux défauts et les défauts généraux. grave défaut est et BPF des médicaments exige un écart grave du produit peut causer un risque de défaut de l'utilisateur. Le principal défaut est un défaut plus de décalage par rapport aux exigences de GMP. Un défaut est généralement dévient des exigences des BPF, mais pas dans la mesure oů des défauts majeurs de graves défauts et des défauts. Pour l'inspection du site de défaut constaté, la rectification de l'entreprise, la rectification en place sinon ŕ court terme, il oblige les entreprises ŕ fournir un plan d'actions correctives ou d'un programme, qui sera soumis ŕ l'achčvement des autorités de réglementation des médicaments de rectification. Si l'inspection sur place a constaté de graves violations des entreprises illégales, seront examinées et traitées selon le département de droit de l'inspection pharmaceutique.
L'inspection spéciale liée ŕ l'information rendue publique par le site Web Drug Administration provinciale du Fujian, Pičces des entreprises de production de la médecine chinoise a inspecté 31 (35 entreprises dans la province, une licence de production arrive ŕ expiration, trois rapports abandonnées), les inspecteurs envoyés 88 les passagers, ont été trouvés dans un des défauts graves, 21 défauts majeurs, 223 défauts généraux. Jusqu'ŕ présent, 28 fabricants de médicaments soumis rapport de rectification, un grave défaut, 18 défauts majeurs, 204 défauts ont rectification générale est terminée, trois défauts majeurs, 26 rectification de défaut général se déroule comme prévu.

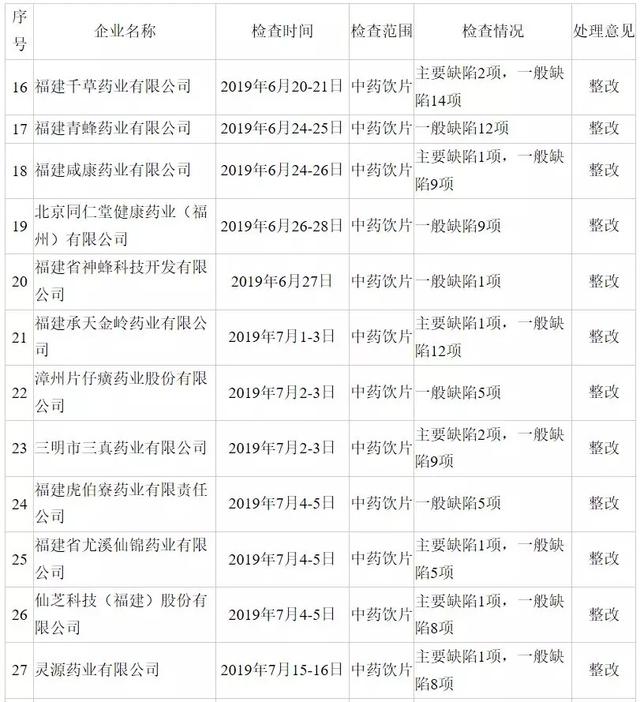

En outre, en raison du Fujian Longhua Pharmaceutical Co., Ltd, Fujian Shankland biologique Technology Co., narcisses Pharmaceutical (Jian'ou) Co., Ltd (anciennement le nouveau Fujian Wuyi Pharmaceutical Co., Ltd.) a été arręté, Wang Min (Xiamen) pharmaceutique limité les licences de production de drogue le 10 Mars, 2019 l'expiration, la province du Fujian et Drug administration de ces quatre sociétés n'a pas vérifié.












